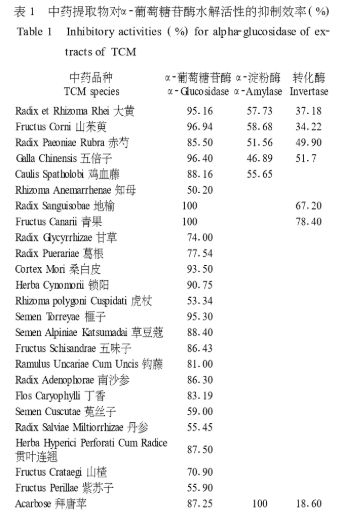
我们共筛选126种常用中药,其中24种中药提取物显著抑制α-葡萄糖苷酶对麦芽糖的水解,占筛选中药的19 %;5种提取物抑制α-淀粉酶对淀粉的水解,占筛选中药的3.97%;6种提取物抑制转化酶对蔗糖的水解﹐占筛选中药的4.76 %(见表1)。阳性药物阿卡波糖对α-淀粉酶的抑制活性很强,对α -葡萄糖苷酶的抑制活性次之,对蔗糖酶的抑制活性很弱,这一结果符合阿卡波糖的作用机理。
供应产品目录:
乙基-2-乙酰氨基-2-脱氧-β-D-吡喃葡萄糖苷 2495-96-7
乙基-2,3,4,6-四-O-乙酰基-α-D-硫代吡喃半乳糖苷 126187-25-5
乙基-2,3,4,6-四-O-乙酰基-α-D-硫代吡喃葡萄糖苷 56245-73-5
乙基-2,3,4,6-四-O-乙酰基-β-D-硫代吡喃半乳糖苷 55722-49-1
乙基2,3,4,6-四-O-乙酰基-β-D-硫代吡喃葡萄糖苷 4160-79-5
乙基-1-硫代-β-D-吡喃半乳糖苷 7473-36-1
乙基-1-硫代-β-D-吡喃半乳糖苷 56245-60-4
乙基-β-D-吡喃葡萄糖苷
2-氟代-2-脱氧-1,3,5-三-O-乙酰基-α-D-呋喃阿拉伯糖 444586-86-1
L-岩藻糖 2438-80-4
荧光素-β-D-吡喃半乳糖苷 102286-67-9
荧光素-二-β-D-吡喃半乳糖苷 17817-20-8
荧光素-二-β-D-吡喃葡萄糖苷 129787-66-2
荧光素-二-β-D-吡喃葡萄糖醛酸甲酯
荧光素-二-2-乙酰氨基-2-脱氧-β-D-吡喃葡萄糖苷
6-氟-3-吲哚基-β-D-吡喃半乳糖苷 207727-11-5
D-果糖-1,6-二磷酸三钠盐 81028-91-3
十七烷基-2-乙酰氨基-2-脱氧-β-D-吡喃葡糖苷 262856-90-6
十七烷基-2,3,4,6-四-氧-乙酰基-β-D-吡喃氨基葡萄糖苷 585.77
七烷基-2-乙酰氨基-2-脱氧-β-D-吡喃葡糖苷 20818-25-1
七烷基-2,3,4,6-四-氧-乙酰基-β-D-吡喃氨基葡萄糖苷 115431-24-8
庚烷基-β-D-吡喃葡萄糖苷 78617-12-6
庚烷基-β-D-硫代吡喃葡萄糖苷 85618-20-8
十六烷基-2-乙酰氨基-2-脱氧-β-D-吡喃葡糖苷 115414-49-8
十六烷基-2,3,4,6-四-氧-乙酰基-β-D-吡喃氨基葡萄糖苷 115414-47-6
十六烷基-β-D-吡喃葡糖苷
十六烷基-β-D-麦芽糖苷 98064-96-1
己基-2-乙酰氨基-2-脱氧-β-D-吡喃葡糖苷 190912-49-3
己基-2,3,4,6-四-氧-乙酰基-β-D-吡喃葡萄糖苷 172945-26-5
己基-β-D-吡喃葡糖苷 59080-45-4
己基-β-D-麦芽糖苷 870287-95-9
己基-β-D-硫代吡喃葡萄糖苷 85618-19-5
4-甲基-6-十六酰氨基香豆素-β-D-吡喃半乳糖苷 94452-17-2
8-羟基喹啉基-β-D-吡喃半乳糖苷 113079-84-8
8-羟基喹啉基-β-D-吡喃葡萄糖苷 29266-96-4
yyp2021.6.30

