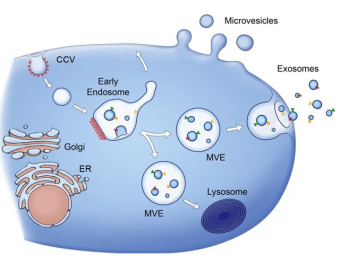
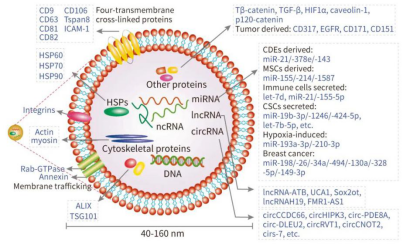
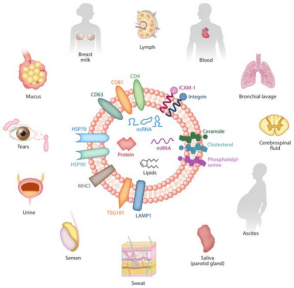
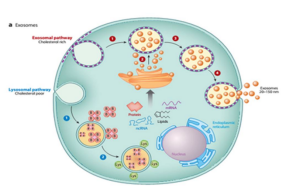
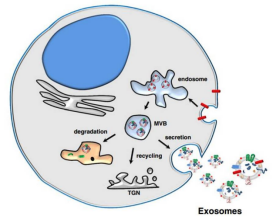
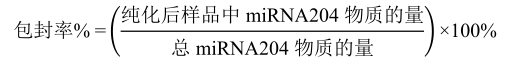干细胞外泌体,是一种能被大多数干细胞分泌的微小囊泡,直径大约在30-150nm,由脂质、蛋白质和核酸组成。外泌体一旦通过胞吐作用从干细胞中释放,复杂的混合因子能作为信号分子传递给其他细胞,从而改变其他细胞的功能。
外泌体被包裹在坚硬的双层膜中,双层膜保护外泌体的内容物,使外泌体能够在组织中长距离移动。干细胞外泌体因在上皮组织的增殖、迁移、再生、炎症和瘢痕控制等方面的作用,有望成为“无细胞的细胞治疗”工具。
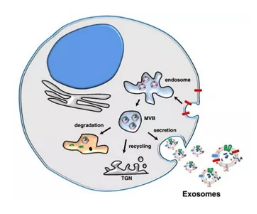
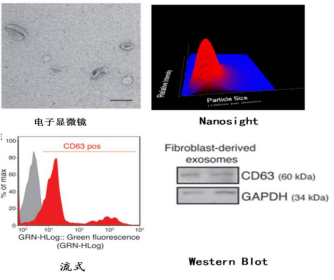
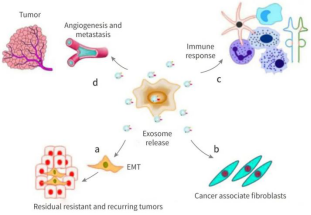
已有研究表明外泌体是干细胞旁分泌作用的主要介质,它们的内容物 (mRNA、microRNA、各种抗凋亡和促血管生成因子)被发现可诱导成纤维细胞的迁移和增殖以及胶原的合成。
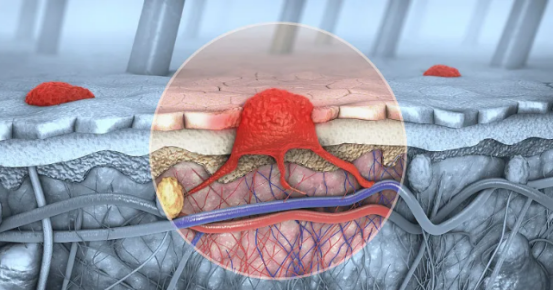
外泌体在创面愈合各个阶段发挥的作用
皮肤创面愈合是一个复杂而精细的过程,大致可分为三个阶段:炎症期、增殖期和重塑期。
在炎症早期,中性粒细胞是重要的细胞,负责吞噬和细胞因子的释放来诱发炎症。在炎症后期,巨噬细胞成为主导细胞类型,并起控制炎症的作用。研究发现,间充质干细胞来源的外泌体可促进受体巨噬细胞向抗炎M2表型转变。它们还能调节B淋巴细胞的活化、分化和增殖,并能抑制T淋巴细胞的增殖。
此外,间充质干细胞衍生的外泌体可以将活化的T淋巴细胞转化为T调节表型,从而发挥免疫抑制作用。用脂多糖预处理间充质干细胞释放富含microRNA let-7b的外泌体,当内化时,let-7b可以通过抑制TLR4/NF-κB通路和激活STAT3/ AKT通路调节巨噬细胞极化。

增殖期开始于受伤后第4天,结束于第20天左右,参与增殖阶段的细胞功能是复杂的,以迁移、增殖、细胞外基质沉积和血管生成为标志,通过不同的机制来实现。干细胞外泌体可以改善皮肤细胞(如成纤维细胞和角质形成细胞)的迁移和增殖。此前有报道,来自人脂肪源间充质干细胞的外泌体可以加速真皮成纤维细胞和角质形成细胞的迁移和增殖,并激活AKT通路。

正常的疤痕是伤口愈合的重塑期。然而,过度瘢痕是由肌成纤维细胞产生的胶原蛋白异常和皮肤功能丧失造成的。研究表明,人羊膜干细胞外泌体也可以通过控制细胞外基质的沉积来减少瘢痕,部分原因可能是通过刺激基质金属蛋白酶-1 (MMP-1)实现的。

人脐带干细胞外泌体在小鼠模型中通过抑制TGF-β/SMAD2途径抑制肌成纤维细胞的分化。这些外泌体内容物中含有的MicroRNAs可能是造成肌成纤维细胞分化的重要原因。
产品/服务供应:
红细胞膜
白细胞膜
血小板细胞膜
细菌细胞膜
肿瘤细胞膜
干细胞膜
原代细胞膜
各种细胞系膜
上皮细胞膜
成纤维细胞膜
生物膜
细胞膜提取
细胞膜提取分离技术
生物仿生膜
血液分泌的外泌体
唾液分泌的外泌体
尿液分泌的外泌体
脑脊液分泌的外泌体
乳汁分泌的外泌体
外泌体的捕获和分离产品
乳胶微球共价结合外泌体marker相关抗体
外泌体试剂产品
外泌体专用培养基
外泌体提取浓缩液
无外泌体胎牛血清
外泌体标志蛋白检测试剂盒
外泌体专用裂解液
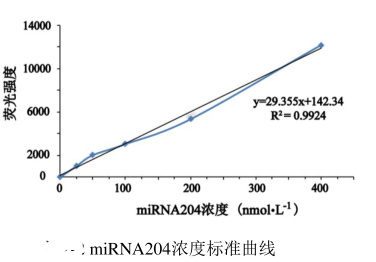
外泌体miRNA检测
外泌体荧光标记染料
外泌体抑制剂
外泌体提取试剂盒试用装
外泌体试剂盒产品
细胞上清外泌体提取试剂盒
血清血浆外泌体提取试剂盒
其他体液外泌体提取试剂盒
多合外泌体提取试剂盒
外泌体提取分离、鉴定、纳米粒子分析
无外泌体血清(Exosome-depleted FBS)
载外泌体水凝胶
外泌体蛋白分析
外泌体多因子检测
磷酸酶通过外泌体影响肿瘤转移
外泌体纯化
外泌体核酸纯化
四次跨膜蛋白外泌体
细胞内的囊泡运输外泌体
直径为30~100 nm细胞外囊泡外泌体
CD9外泌体标志物
CD63外泌体标志物
外泌体超速离心产品
外泌体多聚物沉淀产品
外泌体免疫沉淀产品
脂质双层膜的微小膜泡
外泌体囊泡下游的电镜分析产品
外泌体囊泡NTA分析产品
外泌体囊泡纳米流式(NhaioFCM)分析产品
外泌体囊泡Western Blot分析产品
外泌体囊泡荧光定量(qPCR)分析产品
细胞上清液外泌体提取试剂盒
小鼠调节性树突状细胞(rDC)分泌的外泌体
(regulatory exosomes,rDex)
负载肿瘤抗原的DC外泌体(Dex)
细胞释放的纳米级膜性囊泡外泌体
间充质干细胞(MSC)外泌体
小鼠黑素瘤细胞培养液上清中的外泌体
突变型HIF-1α修饰BMSCs分泌的外泌体
分离纯化肝癌细胞培养液中外泌体
内源性纳米载体外泌体
肿瘤衍生外泌体传递的微RNA
鸟结核分枝杆菌(M.avium)感染巨噬细胞后分泌的外泌体[(+)外泌体
含表皮生长因子受体的外泌体
小鼠肝癌细胞(H22)来源的外泌体(exosomes)
外泌体分离及其蛋白质组学分析
细胞分泌40-100 nm的外泌体
人血清中外泌体(exosome)
Nor-hUC-exo外泌体
IFN-γ-stimulated hUC-exo外泌体
干扰素γ刺激hUC-MSCs分泌外泌体
外泌体表面膜结合型转化生长因子β1( mTGF-β1)
树突状细胞(DC)和肿瘤细胞外泌体
乳腺癌MDA-MB-231细胞中分离外泌体
血清外泌体miR-21
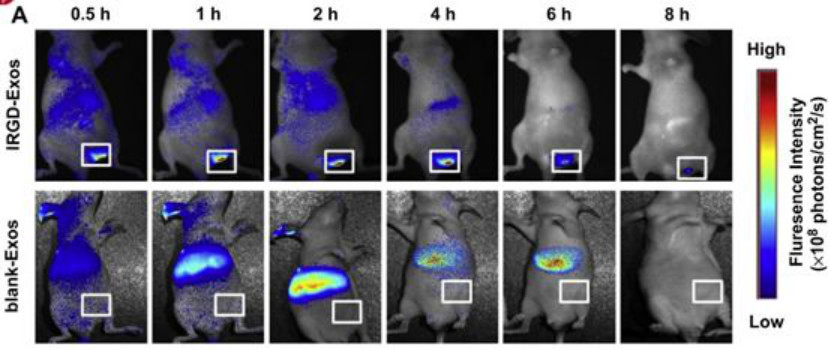
近红外荧光蛋白标记乳腺癌细胞外泌体
外泌体包裹药物载体
(hUC-MSCs)分泌的外泌体(exosomes)
人脐带血树突状细胞(DCs)分泌的外泌体
MDA-MB-231细胞中分离外泌体
iRGD-外泌体-阿霉素
树突状细胞(dendritic cells,DC)外泌体
DC-derived exosome,DCex
外泌体miRNAs
环磷酰胺联合树突状细胞分泌的外泌体
MSCs-derived exosomes,MEX
上述产品与相关检测服务均可提供,仅用于科研研究!
wyf 01.19